Reacción: utilizan CRISPR para proteger de enfermedades cardíacas en ratones
La llamada lesión por isquemia-reperfusión es una de las responsables del daño producido por patologías como el infarto de miocardio. Un trabajo publicado en la revista Science ha empleado los editores de bases, una herramienta de edición genética derivada de CRISPR, para modificar en los corazones de ratones una proteína clave en dicha lesión. Según los autores, la intervención permitió que recuperaran su función tras sufrir un infarto y potencialmente podría emplearse en un amplio abanico de pacientes, pues no depende de la presencia de una mutación concreta.
Lluís Montoliu - CRISPR cardio
Lluís Montoliu
Investigador en el Centro Nacional de Biotecnología (CNB-CSIC) y en el CIBERER-ISCIII
El último día de 2015, tres laboratorios hicieron públicos sus resultados, obtenidos de forma independiente, al usar las herramientas CRISPR de edición genética de primera generación para tratar un modelo de ratón con distrofia muscular de Duchenne, eliminando un fragmento del gen de la distrofina, portador de la mutación causante de la patología. Uno de esos laboratorios era el de Eric N. Olson, del Centro Médico del Sudoeste de la Universidad de Texas, en Dallas, uno de los primeros en demostrar que las CRISPR podían administrarse directamente en animales, encapsuladas en vectores virales, para tratar enfermedades congénitas.
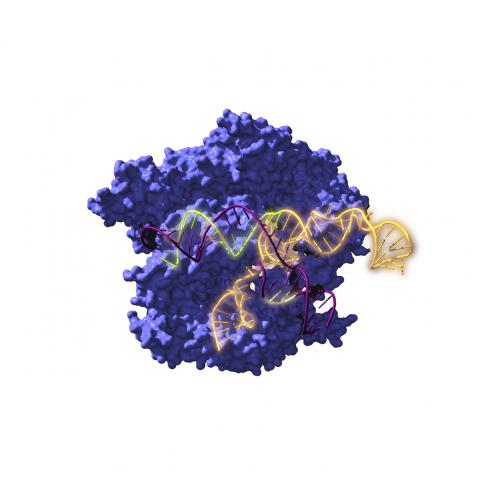
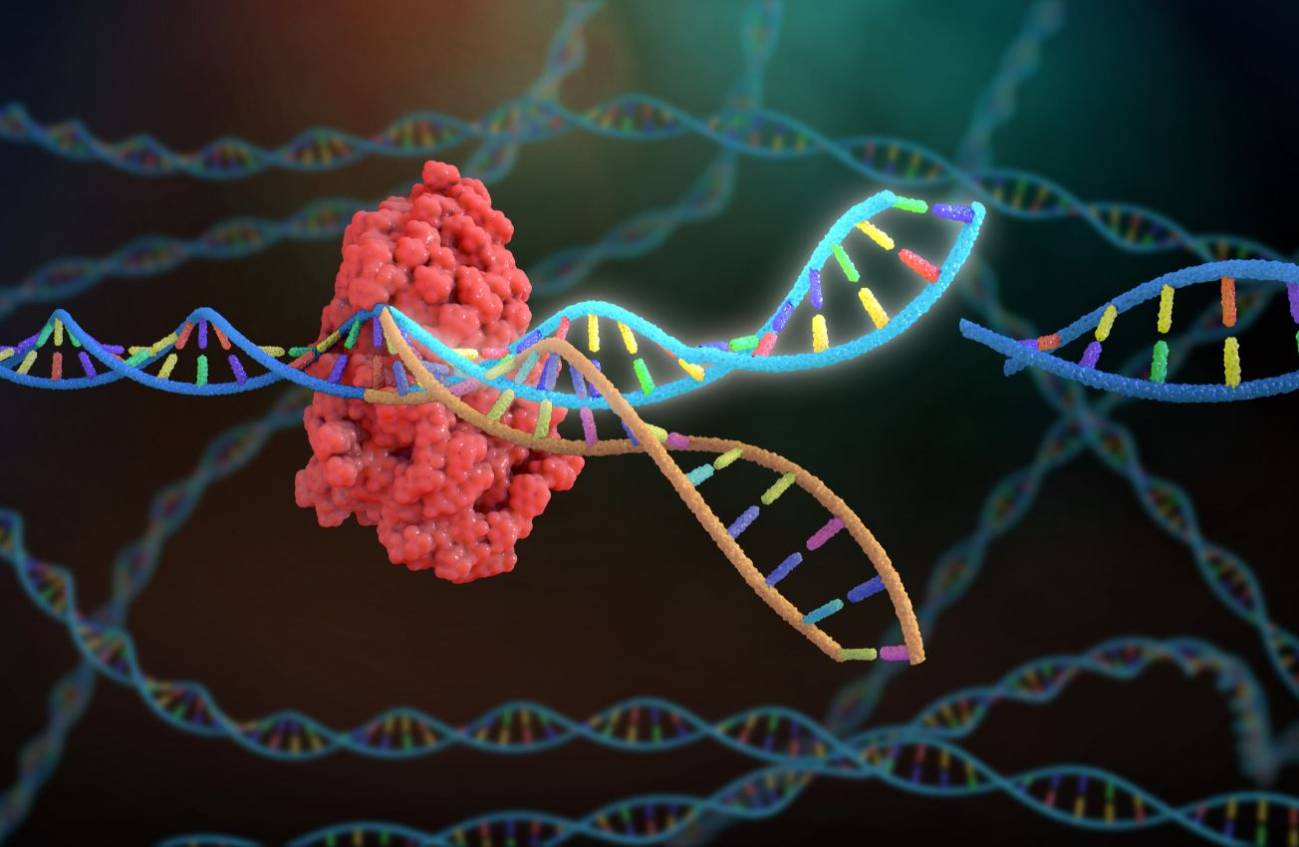
Siete años después, el mismo laboratorio vuelve a sorprendernos con un nuevo uso de las herramientas CRISPR actualmente más evolucionadas, los editores de bases, capaces de cambiar químicamente letras del genoma (por ejemplo, una A por una G) sin cortar el ADN y, por ello, con mayor seguridad. En este trabajo de Lebek y colaboradores, el laboratorio de Olson ha decidido usar un editor de bases para cambiar dos aminóacidos (dos metioninas) de una proteína quinasa llamada CaMKIIdelta, que cuando se oxida y reactiva es causa de enfermedades cardíacas graves. El aminoácido metionina está codificado por el triplete ATG, que los autores cambian a GTG, pasando ahora a codificar el aminoácido valina, el cual ya no puede ser oxidado ni servir para reactivar la proteína.
Prudentemente, los autores evalúan su estrategia primero en células en cultivo, en cardiomiocitos humanos derivados de células pluripotentes inducibles (iPS) y seleccionan los mejores reactivos CRISPR para la edición de bases. Seguidamente, inyectan vectores virales portadores de estos reactivos en el corazón de ratones que han sufrido un infarto cardíaco experimental y observan la recuperación de la función cardíaca. Estas primeras evidencias preclínicas sugieren que algo parecido podría suceder si se inyectaran estos mismos reactivos CRISPR en la zona infartada de un corazón humano, algo que todavía tardará en poder ser investigado. Para ello se necesitan más estudios preclínicos, en animales, que permitan valorar la seguridad y eficacia del procedimiento a corto, medio y largo plazo.
El uso de las herramientas CRISPR no es inocuo. Tampoco lo es el uso de editores de bases. Más allá de las bases que se pretenden modificar, el sistema puede acabar cambiando otras cercanas en la secuencia diana del genoma o en otros genes que presenten secuencias parecidas, compatibles con la guía de ARN que sirve para dirigir los editores de bases al gen seleccionado. Algunas de estas situaciones pueden predecirse con ordenadores. Otras no y deben investigarse experimentalmente. Los autores encuentran modificaciones inesperadas de los dos tipos, en otras bases cercanas a las que quieren modificar del mismo gen y en otros genes similares. Afortunadamente, ellos razonan que ninguna de estas modificaciones no deseadas parece afectar al desarrollo de sus experimentos, pero esto es más producto de la fortuna que de la voluntad de los investigadores. Por ello, hay que seguir investigando editores de bases más optimizados que alteren fundamentalmente las secuencias previstas, sin afectar significativamente otras partes del genoma.
Este nuevo estudio confirma la tendencia observada en los últimos dos años de la rápida evolución de las herramientas CRISPR, con un predominio de los editores de bases (descritos originalmente por David Liu, del Instituto BROAD, en 2016) en las propuestas terapéuticas, por su mayor precisión y seguridad. Sin embargo, como se puede comprobar en este último estudio, todavía no son completas y requieren más investigación.
- Artículo de investigación
- Revisado por pares
- Animales
Lebek et al.
- Artículo de investigación
- Revisado por pares
- Animales