Un ensayo clínico demuestra la eficacia de la vacuna RH5.1/Matrix-M contra la malaria en bebés de Burkina Faso
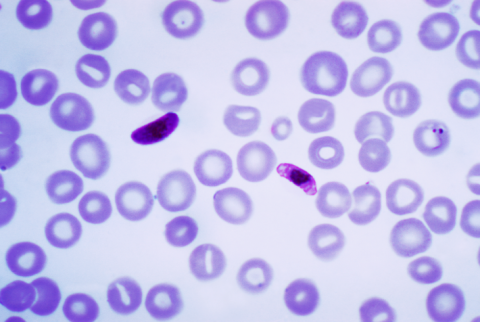
La vacuna RH5.1/Matrix-M es eficaz y segura contra la malaria, según un ensayo clínico de fase 2b realizado con bebés en Burkina Faso, tal y como recoge The Lancet Infectious Diseases. Ya existen otras dos vacunas aprobadas contra la malaria, una enfermedad que causa el parásito Plasmodium falciparum, pero esta actúa en otro momento de la enfermedad: cuando el parásito de la malaria está presente en la sangre. Las otras dos vacunas atacan al parásito cuando se encuentra en el hígado.
241211 vacuna malaria - consuelo ES
Consuelo Giménez Pardo
Profesora titular de la Universidad de Alcalá y vocal de Gestión del Conocimiento e Investigación de Médicos del Mundo
Liderado por el investigador Hamtandi Magloire Natama, se presentan los resultados provisionales realizados en niños de un ensayo de fase IIb, doble ciego, aleatorizado y controlado, sobre la vacuna RH5.1/Matrix M, una vacuna frente a los merozoitos sanguíneos, que parece proveer de una segunda línea de defensa pediátrica frente a la clínica de la malaria. El doctor Magloire Natama –un investigador con experiencia en el estudio de los factores genéticos e inmunológicos que contribuyen a la variación interindividual en la susceptibilidad a la malaria en la primera infancia– fue también coinvestigador y coordinador en el ensayo de fase II de la R21/Matrix-M, segunda vacuna contra la malaria después de la RTS, S/AS02, también preeritrocítica y capaz de actuar frente a otra fase del ciclo biológico del parásito: los esporozoitos.
El ensayo propuesto se ha llevado a cabo en un estudio controlado en niños de 5-17 meses en la región de Nanoro (Burkina Faso), administrando la vacuna durante la temporada de transmisión de la malaria. En el trabajo, que publica The Lancet Infectious Diseases, se indica que RH5.1/Matrix M es segura y bien tolerada y que en tres dosis proporciona anticuerpos anti-RH5.1. Los autores proponen que, como estrategia prometedora en esta segunda generación de vacunas pediátricas frente a la malaria, deberá aplicarse de manera sinérgica en combinación con las vacunas preeritrocícas ya existentes
241211 vacuna malaria - carlota ES
Carlota Dobaño
Profesora de investigación y jefa del Grupo de Inmunología de la Malaria en el Instituto de Salud Global de Barcelona (ISGlobal)
Se trata de un ensayo clínico aleatorizado, controlado y a doble ciego, que es la metodología en epidemiología más robusta que existe, aunque los resultados son todavía preliminares de un análisis interino y hay que esperar al análisis final definitivo para tener estimación más precisa de la eficacia de la vacuna.
Es la primera vez que una vacuna de la malaria basada en un antígeno de la fase sanguínea del parásito (la que causa los síntomas de la enfermedad y la patología) en concreto la proteína de Plasmodium falciparum Rh5, junto con el adyuvante ya usado en otras vacunas (R21: MatrixM) y en covid-19, demuestra eficacia significativa en niños africanos, sin depender de la cepa con que se ha vacunado. La vacuna es segura, genera elevados anticuerpos neutralizantes y es eficaz frente a la malaria en un periodo de seis meses, con un 55 %, que es equivalente a lo que mostró RTS,S en esta misma edad en el ensayo de fase 3 para su registro. También aporta la opción de variar (retrasar) los periodos de tiempo o intervalos de vacunación entre las dosis para mejorar la potencia de la vacunación.
Los resultados se tienen que confirmar en otras zonas endémicas de malaria donde la transmisión no sea tan marcadamente estacional. Además, los intervalos de confianza de la eficacia de la vacuna son amplios y, por tanto, la estimación no es todavía precisa. Se tiene que hacer todavía un seguimiento más largo en los niños para evaluar la duración de dicha protección dado que una de las principales limitaciones de las actuales vacunas es su longevidad en el tiempo, que hay que mejorar para evitar tener que dar dosis de refuerzo.
Es una vacuna prometedora para poder combinar con las dos vacunas de malaria existentes (RTS,S o R21) que se basan en las fases presanguíneas o hepáticas y que no previenen totalmente la infección de la malaria de manera total. Por tanto, la combinación de ambos tipos de vacunas parcialmente protectoras podría llevar a una vacuna multivalente más potente. También indica que retrasar la tercera dosis de vacunación podría beneficiar la respuesta del sistema inmune, viendo que dio lugar a mejor respuesta de anticuerpos y mayor eficacia.
Para contexto adicional, podéis mirar el comentario que hicimos del trabajo previo de este grupo con esta vacuna, que aún no mostraba eficacia.
- Artículo de investigación
- Revisado por pares
- Ensayo clínico
- Humanos
Hamtandi M Natama et al.
- Artículo de investigación
- Revisado por pares
- Ensayo clínico
- Humanos