Reacciones a los resultados del ensayo en fase 3 de la vacuna R21 contra la malaria
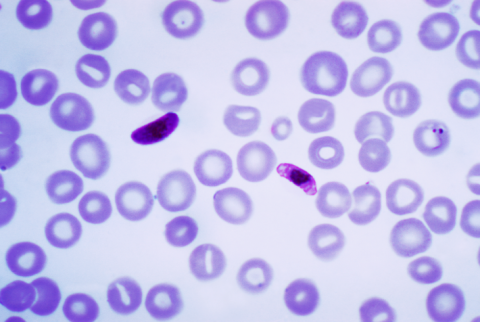
En un ensayo clínico con cerca de 5.000 niños y niñas de entre 5 y 36 meses de edad, una nueva vacuna frente a la malaria —llamada R21/MatrixM— redujo los casos sintomáticos entre un 68 y un 75 % durante el año siguiente. Según los autores, la vacuna será de bajo coste y podría contribuir a reducir sustancialmente el sufrimiento y las muertes por malaria en el África subsahariana. Los resultados de la fase 3 del ensayo se publican en la revista The Lancet.

Jaime J - Malaria
Jaime Jesús Pérez Martín
Especialista en Medicina Preventiva y Salud Pública, subdirector general de Salud Pública de la Región de Murcia y presidente de la Asociación Española de Vacunología (AEV)
Es un estudio excelente, un ensayo clínico realizado en cuatro países africanos con un tamaño muestral de casi 5.500 niños.
Por un lado, esta vacuna tenía resultados publicados de ensayos clínicos fase 2 y los resultados eran concordantes. Además, como los autores dicen, la vacuna ya está autorizada por la OMS y en varios países africanos ha comenzado su uso. Los datos son también concordantes con los de otra vacuna ya en uso frente a la malaria, en concreto Mosquirix, que fue la primera vacuna autorizada frente a la malaria, por lo que con esta nueva vacuna ya tenemos dos. Como novedad más importante está que los datos de eficacia aumentan respecto a los obtenidos por Mosquirix, que tiene cifras de entre el 45 y 55 % de protección. Aquí aumentamos hasta entre el 70 y el 80 %, es decir, ofrece una mejora notable en cuanto a la protección.
Por lo tanto, como novedades aporta una mayor protección y, al mismo tiempo, va a permitir unos programas de vacunación más extensos frente a la malaria de los que contábamos hasta ahora, ya que se dispondrá de una segunda vacuna que tiene un gran número de dosis preparadas para su uso. También como ventaja añadida podríamos tener un aumento de la duración de la protección.
Además, la vacuna usa un nuevo adyuvante, Matrix-M, que hasta ahora no ha estado en uso pero que se puede configurar como un adyuvante muy prometedor para su uso en numerosas vacunas. En nuestro país este adyuvante solo se ha usado en las vacunas frente a la covid de Novavax, pero por desgracia hemos tenido pocas disponibles, por lo que nuestra experiencia con dicho preparado es limitada. Esperemos que los beneficios de este adyuvante se puedan confirmar en otras vacunas.
En cuanto a las limitaciones, están las que dan los propios autores, como el hecho de no medir la eficacia frente a mortalidad, pero eso es muy difícil en un ensayo clínico porque lógicamente son situaciones ideales en las que hay que poner el tratamiento de forma temprana. Sin embargo, midiendo la eficacia frente a la enfermedad luego en la vida real conseguiremos reducciones importantes de mortalidad, por lo que no creo que sea una limitación importante.
Consuelo - Malaria RS
Consuelo Giménez Pardo
Profesora titular de la Universidad de Alcalá y vocal de Gestión del Conocimiento e Investigación de Médicos del Mundo
La historia de la búsqueda de vacunas en la malaria es un camino largo, lleno de aciertos y desaciertos, pero totalmente necesario en la lucha contra el paludismo en su forma más grave. De hecho, la comunidad internacional lleva décadas realizando esfuerzos en la eliminación de esta enfermedad parasitaria y esto ha supuesto importantes cambios en las estrategias de salud pública adoptadas por los países que la padecen. La vacunación es una de las estrategias fundamentales para el control de las enfermedades infecciosas y la disponibilidad de vacunas seguras que proporcionen una protección duradera contra la malaria supone un importante avance en la lucha contra el paludismo. Sin embargo, debe ser estudiada en el contexto de la aplicación de otras intervenciones efectivas, como son el uso de mosquiteras tratadas con insecticida y el acceso a diagnóstico y tratamientos combinados con artemisinina.
Para implementar la vacunación deben considerarse factores como la carga de la enfermedad, el coste-efectividad de la intervención y la cobertura de otras intervenciones destinadas al control y eliminación de la malaria. Por lo tanto, la vacunación debe ser una intervención más a integrar en las estrategias de control y eliminación de esta parasitosis, según el contexto de cada entorno y sistema de salud.
Las vacunas que poseen una mayor eficacia demostrada actúan en la fase preeritrocítica a través de la inoculación de esporozoítos atenuados, que disponen de una mayor eficacia demostrada, pero resultan de difícil aplicación en zonas endémicas debido a sus condiciones de conservación y administración (intravenosa y con dosis frecuentes).
También tenemos las vacunas de subunidad. En el mercado tenemos disponible la RTS,S/AS01E, con una eficacia demostrada limitada pero de más fácil aplicación y conservación, y recientemente la OMS ha recomendado la vacuna R21 para la prevención de la malaria en niños.
En este sentido, ya en el año 2016 se publicaron los resultados del estudio de una vacuna más inmunogénica que la RTS,S que también actúa sobre la proteína circumsporozoíto (PCS). Está desarrollada a partir de antígenos de superficie del virus de la hepatitis B, lo que lleva a una mayor proporción de PCS en la composición de la vacuna. La vacuna ya demostró inmunogenicidad en ratones a dosis muy bajas.
El actual estudio de Datoo et al (2024) continua con los trabajos publicados en Lancet ya realizados publicados en 2021 y 2022. En este caso, en fase 3 del ensayo se muestra una eficacia del 75 % frente a la clínica de la malaria en lugares con malaria estacional y un 67 %, en lugares con malaria habitual, en niños de 5 a 36 meses y, si bien parece haber una disminución de la eficacia en periodos de 3 meses, durante los 12 primeros meses la eficacia permanece por encima del 60 %. En el ensayo de doble ciego realizado en un año en diferentes áreas de Burkina Faso, utiliza un grupo control al que se le aplica la vacuna de la rabia, cuestión que según otros estudios parece proteger frente a la meningitis. En este caso, a pesar de las limitaciones del estudio, los autores proponen que la R21/Matrix-M es capaz de producirse en términos de 100-200 millones de dosis anuales con un coste inferior a 4 dólares por dosis y que puede ayudar a prevenir la malaria.
Lo cierto es que la demanda de vacunas antipalúdicas nunca había sido tan grande y, sin embargo, las existencias de la vacuna ya comercializada, RTS,S son limitadas. Ahora, con la vacuna R21/Matrix-M en la lista de vacunas contra el paludismo recomendadas por la OMS, se espera que el suministro sea suficiente para inmunizar a todos los niños que viven en zonas donde esta enfermedad es un riesgo para la salud pública. En este sentido se plantea como costo-eficaz e inocua, de manera que la elección de una u otra vacuna se realizará en cada país según las características de los programas, del suministro de vacunas y de su asequibilidad. Como se hace con otras vacunas nuevas, se seguirá vigilando su posible toxicidad.
El principal desafío al que se enfrenta la vacuna contra la malaria es la integración de la vacunación en el sistema de salud, como intervención en la estrategia para el control y eliminación de la malaria. Así, debería poder integrarse en el calendario vacunación que ya está en funcionamiento.
Pero en vacunas de malaria, no hay panaceas. Hay que tener en cuenta que en las vacunas de subunidad la eficacia demostrada es reducida y se limita al rango de entre 5 y 7 meses de edad, para los adultos estas cifras disminuyen a 34 % de eficacia, además de que, según la evidencia disponible no parece que la protección se prolongue en el tiempo, por lo que los niños vacunados estarían de nuevo expuestos a la malaria desde muy corta edad.
En líneas generales, los esfuerzos deberían encaminarse a mejorar las capacidades, tanto en recursos humanos como en infraestructuras, para monitorear y gestionar de forma eficiente las resistencias a los insecticidas, así como para disponer de nuevos productos (insecticidas, tratamientos y vacunas) adecuados y accesibles, útiles en el control de la malaria.
Dobaño - Malaria
Carlota Dobaño
Profesora de investigación y jefa del Grupo de Inmunología de la Malaria en el Instituto de Salud Global de Barcelona (ISGlobal)
Los ensayos clínicos de fase 3 para registro de una vacuna, como este, son estudios ejecutados con mucho rigor y bajo monitorización externa, y el diseño y desempeño está bajo escrutinio de comités expertos de la OMS antes de recomendar esta vacuna R21 y por revisores externos de la revista Lancet. Por tanto, el estudio es en general de calidad, aunque con ciertas limitaciones que se mencionan en la discusión y comento abajo
El estudio demuestra la utilidad de una segunda vacuna para la malaria desarrollada en Oxford, con una formulación muy parecida a la primera vacuna que la OMS recomendó tras otro ensayo multicéntrico más amplio de fase 3 y una serie de estudios piloto de implementación en tres países africanos (RTS,S/AS01E o Mosquirix de GSK). Ambas constan de un antígeno frente al parásito de la malaria basado en la proteína del circumsporozoito, de la superficie del Plasmodium falciparum que inyecta el mosquito transmisor, fusionado al antígeno de superficie del virus de la hepatitis B y formulado con un adyuvante que estimula una respuesta inflamatoria por parte del sistema inmunitario innato, e inducen niveles elevados de anticuerpos frente al parásito.
La vacuna muestra una eficacia elevada en áreas de malaria estacional cuando es administrada justo antes de los meses de lluvias asociados a la alta transmisión de la infección, y menos eficacia en los lugares de transmisión menos intensa y perenne. Los autores indican que se podrá producir de manera económica un elevado número de dosis de vacuna, lo que beneficiará que un mayor número de niños africanos la reciban, dada la actual limitación a nivel de manufactura de la otra vacuna disponible. Igual que ha ocurrido con la pandemia de covid-19, el hecho de disponer de más de una vacuna posibilita una cobertura mayor. Ambas vacunas se consideran de primera generación, con eficacias mejorables, y se necesita seguir investigando brechas del conocimiento (por ejemplo, por qué no protege al 90-100 % de los niños) para poderlas optimizar en segundas generaciones.
Se tiene que monitorizar todavía la duración de la eficacia de dicha vacuna para evaluar más extensamente su impacto en salud pública, así como su eficacia en zonas de África donde hay una elevada transmisión de la malaria y todo el año. Los dos centros del África del Este incluidos tienen muy baja transmisión de malaria en la actualidad y no son completamente representativos de la epidemiología que existe en gran parte de las zonas endémicas del continente, donde la malaria es una de las primeras causas de enfermedad y mortalidad de su población.
- Artículo de investigación
- Revisado por pares
- Aleatorizado
- Ensayo clínico
- Humanos
Datoo et al.
- Artículo de investigación
- Revisado por pares
- Aleatorizado
- Ensayo clínico
- Humanos