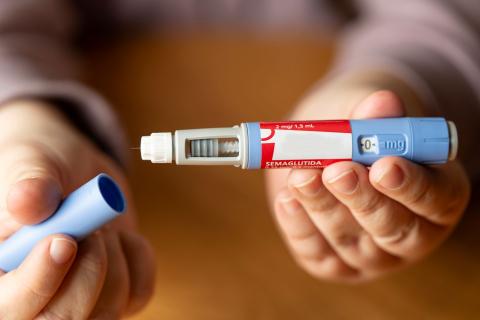
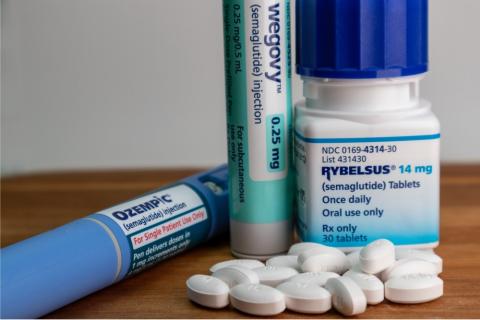
La semaglutida oral no frena la progresión del alzhéimer, según un ensayo
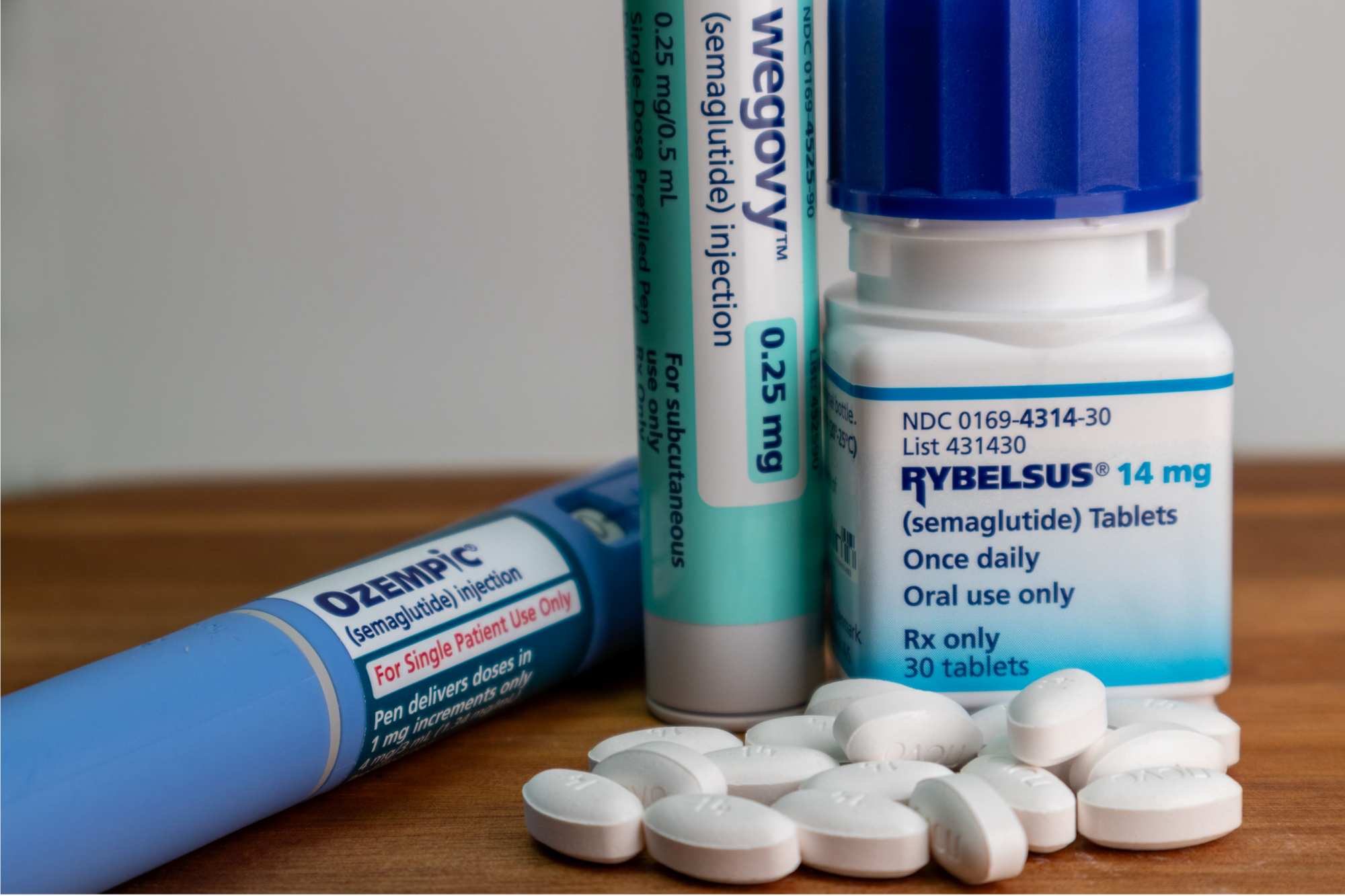
La semaglutida oral no es eficaz para ralentizar la progresión en pacientes con enfermedad de Alzheimer leve, según concluyen los primeros grandes ensayos clínicos aleatorizados de fase 3 publicados en The Lancet. En estos ensayos, unos 3.800 pacientes de entre 55 y 85 años con un diagnóstico confirmado y síntomas leves recibieron hasta 14 mg diarios de semaglutida oral o un placebo. Tras dos años, no se observó ninguna diferencia significativa en la progresión de la enfermedad.
Cristóbal Morales - semaglutida alzhéimer
Cristóbal Morales
Responsable de la Unidad Salud Metabólica, Diabetes y Obesidad Hospital Vithas Sevilla y vocal de la Sociedad Española para el Estudio de la Obesidad (SEEDO)
Aquí la noticia sería que no se ha conseguido el objetivo primario, el efecto beneficioso, como ha ocurrido con semaglutida en otras indicaciones. La noticia sería la falta de resultados positivos, lo cual no lleva a desmontar la hipótesis. Seguimos pensando que la neuroinflamación, esa inflamación crónica de bajo grado, pudiese tener un valor en enfermedades como el alzhéimer. En datos experimentales parecía que se apuntaba así.
Por esa hipótesis fue por lo que se lanzó este ensayo clínico, en el cual no se ha demostrado el beneficio. Este estudio clínico era población con enfermedad de Alzheimer inicial, pero con una baja proporción de diabetes y una baja proporción de obesidad. Tenemos que seguir investigando es esta enfermedad tan prevalente.
La ciencia se construye a través de errores y también los resultados negativos son positivos. Quizás deberemos evaluar si en personas con diabetes, con alto riesgo cardiovascular y con inflamación crónica de bajo grado, este tipo de tratamiento pudiese tener algún valor.
En resumen, esto es simplemente un resultado, un dato que nos tiene que hacer seguir investigando con la hipótesis de la neuroinflamación para explorar si hubiese posibles soluciones que pudiesen beneficiar a tanta población con esta enfermedad.
Diego Bellido - semaglutida alzhéimer
Diego Bellido
Jefe del Servicio de Endocrinología y Nutrición en el Complejo Hospitalario de Ferrol (CHUF) y presidente de la Sociedad Española de Obesidad (SEEDO)
¿La nota de prensa refleja el estudio con precisión?
“Sí, en lo esencial sí. Transmite correctamente que la semaglutida oral no frenó la progresión clínica del alzhéimer precoz, aunque hubo cambios en biomarcadores que no se tradujeron en beneficio clínico. El posible sesgo está en simplificar demasiado esos matices”.
¿El estudio es de buena calidad?
“Sí. Es un trabajo metodológicamente robusto: dos ensayos fase 3, aleatorizados, doble ciego, controlados con placebo, con 3.808 participantes en 566 centros de 40 países. La conclusión principal está bien sustentada porque el desenlace primario fue claramente negativo en ambos ensayos”.
¿Cómo encaja este trabajo con la evidencia existente?
“Encaja como un estudio que corrige el entusiasmo previo. La evidencia preclínica, observacional y algunos estudios pequeños sugieren beneficio potencial de los agonistas GLP-1, pero este ensayo grande no confirma eficacia clínica en alzhéimer precoz”.
¿Han tenido en cuenta los autores los factores de confusión? ¿Hay limitaciones importantes?
“Sí, razonablemente. Ajustaron variables relevantes en el análisis y el diseño fue sólido. Aun así, hay limitaciones: más abandonos por efectos adversos en el grupo de la semaglutida, posible desenmascaramiento [del ciego] por efectos gastrointestinales y pérdida de peso, y el subestudio de LCR fue mucho más pequeño que el ensayo principal”.
¿Cuáles son las implicaciones para el mundo real?
“La implicación práctica es clara: estos datos no apoyan usar semaglutida oral de 14 mg para frenar el alzhéimer precoz. Puede seguir siendo útil en obesidad o diabetes, pero no debe extrapolarse su beneficio al tratamiento modificador de la enfermedad de Alzheimer”.
Xavier Morató - semaglutida alzhéimer
Xavier Morató
Director de ensayos clínicos de Ace Alzheimer Center Barcelona
Los estudios EVOKE y EVOKE+ se basaron en la hipótesis de que el impacto mediado por semaglutida sobre la neuroinflamación podría reducir la progresión de la enfermedad en pacientes con enfermedad de Alzheimer (EA). Evidencia del mundo real con semaglutida indicó que su uso en pacientes con diabetes tipo 2 se asociaba con un menor riesgo de demencia, lo que sugiere posibles efectos neuroprotectores más allá del control glucémico. Estos hallazgos proporcionaron una base importante para investigar más a fondo la semaglutida como una estrategia para reducir el riesgo de demencia.
Las condiciones metabólicas en la mediana edad, como la obesidad y la diabetes, son factores de riesgo bien establecidos y modificables para el desarrollo de demencia (Comisión Lancet sobre factores de riesgo de demencia). El exceso de adiposidad y la alteración del metabolismo de la glucosa contribuyen a la inflamación crónica, la disfunción vascular y otros mecanismos fisiopatológicos implicados en la neurodegeneración y el deterioro cognitivo. En conjunto, esta evidencia respalda la evaluación de la semaglutida como un enfoque terapéutico para mitigar el riesgo de demencia y mejorar la salud cerebral a largo plazo.
En los estudios EVOKE, la edad media fue de 72,2 años. Podría plantearse la hipótesis de que estas intervenciones deberían aplicarse en etapas más tempranas de la vida. En paralelo, dado que no todos los participantes toleraron la dosis más alta de 14 mg y, en consecuencia, recibieron 3 o 7 mg durante el estudio, una mejor comprensión de la correlación entre las dosis y los cambios en los biomarcadores de la enfermedad de Alzheimer permitiría interpretar mejor los resultados. La dosis oral de 14 mg es equivalente a la administración subcutánea semanal de 0,5 mg. Finalmente, estos pacientes eran positivos para amiloide, y podría ser necesario combinar la eliminación de amiloide con el tratamiento con agonistas de GLP-1 para observar un efecto. Alternativamente, estos tratamientos podrían ser eficaces en etapas más tempranas, en pacientes con mayor riesgo de acumulación de amiloide, antes de que el amiloide y la tau se acumulen en el cerebro.
- Artículo de investigación
- Revisado por pares
- Aleatorizado
- Ensayo clínico
- Humanos
Cummings et al.
- Artículo de investigación
- Revisado por pares
- Aleatorizado
- Ensayo clínico
- Humanos