Reacciones: un gel detiene tumores cerebrales en ratones
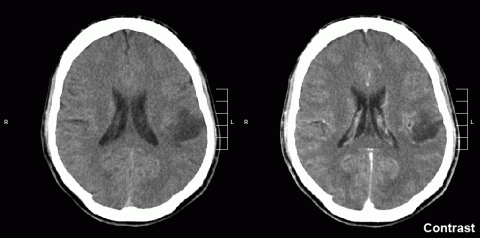
Un fármaco en forma de gel curó al cien por cien de los ratones con un tumor cerebral muy agresivo. Los autores confían es que sea un primer paso para ayudar a pacientes humanos con glioblastoma, uno de los tumores cerebrales más peligrosos en seres humanos. El artículo se publica hoy en PNAS.
Jordi Bruna - reacción gel tumor
Jordi Bruna Escuer
Coordinador de la Unidad de Neurooncología del Institut d'Investigació Biomèdica de Bellvitge (IDIBELL) e investigador del Grupo de Neuroplasticidad y Regeneración de la Universitat Autònoma de Barcelona
El modelo animal en que se basa el estudio no es nada representativo de lo que es un glioblastoma humano. Han trabajado con una línea celular murina a la que químicamente se le indujo una serie de alteraciones que mimetizan morfológicamente al glioblastoma, pero que a nivel molecular no tienen nada que ver con el glioblastoma humano. Suele utilizarse para estudiar los efectos de la inmunidad del huésped. Pero afirmar que la reacción inmunitaria del ratón ante este glioma experimental sea la misma que presenta el paciente es un salto de fe más que considerable. Queda un trecho importante para que la terapia que proponen pueda ser testada en pacientes para valorar primero seguridad y después algún tipo de eficacia.
gel glioblastoma - Pilar Sánchez Gómez
Pilar Sánchez Gómez
Investigadora titular en el Instituto de Salud Carlos III, jefa de la Unidad de Neurooncología en la Unidad de Investigación en Enfermedades Crónicas (UFIEC-ISCIII)
Un grupo de investigadores de la Universidad Johns Hopkins, en colaboración con otros centros, ha encontrado una forma de terapia que es capaz de erradicar gliomas agresivos en modelos de ratón. Estos gliomas agresivos, también llamados glioblastomas, tienen muy mal pronóstico. Los pacientes con este tipo de tumores son sometidos a cirugía con el fin de eliminar la mayor cantidad posible de tumor. Posteriormente se les administran varios ciclos de radioterapia, combinada con quimioterapia con un agente denominado temozolomida. A pesar de este tratamiento agresivo, el tumor siempre vuelve a crecer y la supervivencia de los pacientes es muy baja (en torno al 5 % de supervivencia 5 años después del diagnóstico).
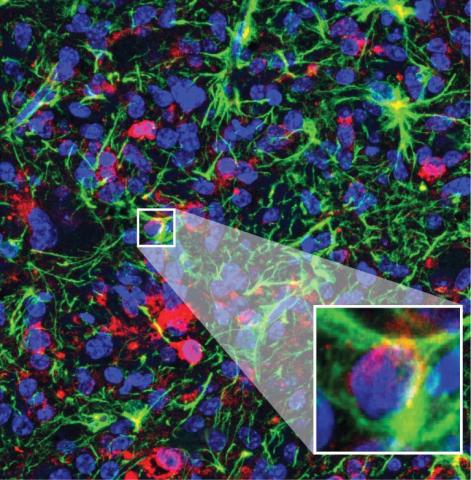
En este estudio los investigadores han diseñado una estrategia para liberar el fármaco antitumoral directamente en la cavidad quirúrgica, para conseguir que llegue de manera más eficiente al cerebro. Para ello utilizan un hidrogel que contiene un fármaco dirigido a frenar el crecimiento de las células tumorales, junto con una proteína destinada a favorecer que las células inmunes del propio paciente se activen y sean capaces de atacar el tumor. Con esto último pretenden que la terapia sea más efectiva y, sobre todo, más duradera. Esta estrategia la prueban en un modelo de glioblastoma en ratón muy utilizado por los investigadores, el modelo de la línea GL261, al que someten a ‘cirugía’ para después depositar el hidrogel con el fármaco. Aunque otros investigadores han publicado diferentes moléculas capaces de frenar el crecimiento de estos tumores, es cierto que el resultado que los investigadores muestran en este artículo es espectacular, ya que son capaces de erradicar totalmente las células tumorales. Son capaces, por tanto, de curar a los animales, lo cual es difícil porque se trata de una línea celular muy agresiva.
Uno de los hándicaps en el tratamiento de los pacientes con tumores cerebrales y, concretamente, con glioblastomas es la dificultad para que el fármaco llegue al cerebro. Hace varios años ya hubo algunos ensayos clínicos usando Gliadel, que consistía en unas pastillas de liberación de fármaco que se depositaban en la cavidad de la cirugía. De hecho, la Universidad Johns Hopkins y, en concreto, algunos de los investigadores del presente estudio, participaron en dichos ensayos. Aunque Gliadel no demostró ser eficaz en pacientes con glioblastomas, los grandes avances que ha habido en el conocimiento de la biología de los estos tumores, junto con las mejoras en el diseño de los geles para liberar fármacos, permiten ser optimista en cuanto a ensayos clínicos futuros.
Entre las limitaciones del estudio destacan dos: por un lado, que los investigadores no consiguen discernir qué parte del efecto antitumoral se debe a la presencia del agente antitumoral y cuánto a la activación de la respuesta inmune. Por otro lado, los investigadores utilizan un único modelo de glioblastoma que, aunque se utiliza mucho en el campo de la neurooncología, ha sido criticado por no representar fielmente la biología de estos tumores, particularmente, en lo que se refiere a su interacción con las células inmunes. Es por ello que todavía deben realizar ensayos con otros modelos, ya sea de ratón o en modelos más cercanos a la clínica, antes de pensar en diseñar ensayos clínicos en pacientes.
- Artículo de investigación
- Revisado por pares
- Estudio experimental
- Animales
Wang et al.
- Artículo de investigación
- Revisado por pares
- Estudio experimental
- Animales